Антрациклины представляют собой класс химиотерапевтических средств, эффективных при лечении многих форм рака, включая лейкемию, лимфому и рак молочной железы. Антрациклины, такие как доксорубицин, часто используемый против рака молочной железы, убивают раковые клетки, повреждая их ДНК. Однако эти эффективные химиотерапевтические препараты также вызывают токсические эффекты в сердце примерно у десяти процентов пациентов, что в конечном итоге может привести к сердечной недостаточности, особенно у пожилых пациентов с ранее существовавшими сердечно-сосудистыми заболеваниями.
В настоящее время врачам не хватает надежных стратегий для прогнозирования того, какие пациенты подвержены риску этого связанного с антрациклинами повреждения сердца, называемого кардиотоксичностью, снижения функции сердца, которое может привести к сердечной недостаточности , или для выявления его на самых ранних стадиях.
Теперь команда под руководством исследователей из Медицинского центра Бет Исраэль Диаконисс (BIDMC) идентифицировала белок, связанный с возникновением сердечной токсичности, связанной с антрациклином. В двух исследованиях, проведенных с участием женщин, проходящих лечение от рака молочной железы , уровни белка, известного как гемопексин, циркулирующего в крови, были связаны с повышенной сердечной токсичностью. Последующие исследования на мышах показали, что белок обладает защитными свойствами для сердца.
Эти результаты, опубликованные в Science Advances , предполагают, что организм вырабатывает белок в качестве защитной меры против сердечной токсичности, вызванной терапией. Если это так, клиницисты могут однажды использовать этот белок для мониторинга пациентов, проходящих лечение рака антрациклином, на наличие признаков аномальной сердечной функции с помощью простого анализа крови.
«Учитывая растущее бремя как сердечной недостаточности, так и рака среди стареющего населения, разработка новых биомаркеров и стратегий защиты сердца имеет важное значение для минимизации воздействия сердечной токсичности, связанной с терапией рака», — сказал старший и соответствующий автор Аарти Аснани, доктор медицинских наук. , кардиолог и директор программы кардиоонкологии в BIDMC. «Это исследование идентифицирует индукцию циркулирующего гемопексина как сердечно-защитный механизм, относящийся к пациентам, получающим антрациклины».
Аснани и его коллеги изучили 30 женщин с диагнозом рак молочной железы , которым было назначено лечение антрациклиновой химиотерапией. У участников был анализ крови и другие данные, собранные на исходном уровне, до того, как они получили режим доксорубицина. Анкеты, образцы крови и эхокардиограммы получали каждые три месяца в течение периода исследования.
Через три месяца после начала лечения рака ученые увидели общее снижение сердечной функции в когорте участников: у шести пациентов в течение года развились симптомы сердечной недостаточности. За это время исследователи отслеживали 1317 белков, циркулирующих в плазме крови участников. Команда наблюдала изменения в общей сложности 39 белков, при этом увеличение количества гемопексина наиболее сильно ассоциировалось с ранней сердечной токсичностью. Второе исследование с группой из 31 женщины дало почти идентичные результаты.
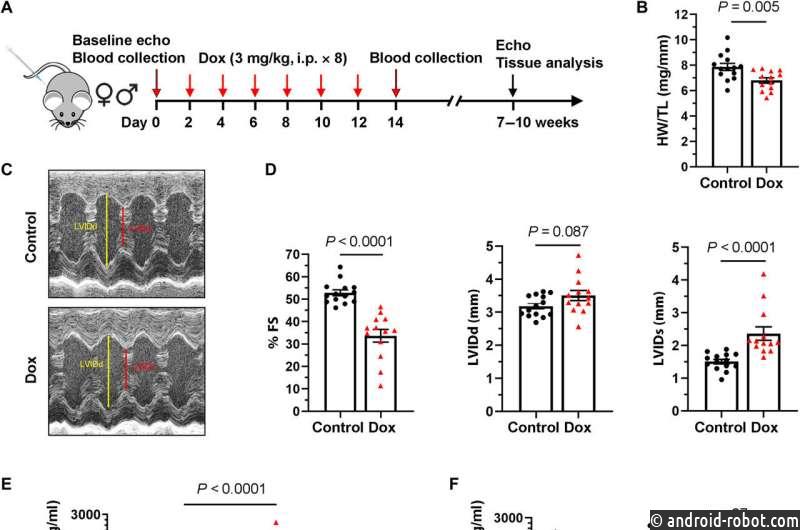
«Основываясь на этих данных, полученных на людях, мы использовали модель мыши, которая точно отражала проблемы с сердцем, наблюдаемые у пациентов, получавших доксорубицин», — сказал первый автор Цзин Лю, доктор медицинских наук, постдокторский исследователь в Отделе сердечно-сосудистой медицины. на БИДМК. «Как мы видели у пациентов, уровень гемопексина в плазме у мышей был повышен в течение 24 часов после завершения химиотерапии и был тесно связан с последующей сердечной функцией».
Установив четкую связь между сердечной токсичностью, вызванной антрациклином, и повышением уровня гемопексина, ученые попытались определить функциональную роль гемопексина. Когда исследователи лечили лабораторных мышей дикого типа (нормальных) доксорубицином, они обнаружили, что введение гемопексина предотвращает развитие сердечной дисфункции.
Однако, когда они провели аналогичный эксперимент на генетически измененных мышах, у которых отсутствует встречающийся в природе белок гемопексина, мыши с дефицитом гемопексина продемонстрировали повышенную сердечную токсичность доксорубицина по сравнению с мышами дикого типа. Полученные данные свидетельствуют о том, что организм может вырабатывать гемопексин в качестве защитной реакции на вызванное антрациклином повреждение сердца.
«Эти результаты служат основой для будущих исследований по разработке гемопексина как биомаркера и защитной терапии для пациентов с риском сердечной токсичности, связанной с химиотерапией», — сказал Аснани, который также является ассоциированным членом Исследовательского института рака в BIDMC. «Сейчас мы работаем над тем, чтобы выяснить, применимы ли наши результаты к большей группе пациентов разного пола и других типов рака, таких как лимфома».