Исследователи Медицинской школы Университета Индианы изучают, как дефицит гена в иммунных клетках может влиять на прогрессирование болезни Альцгеймера.
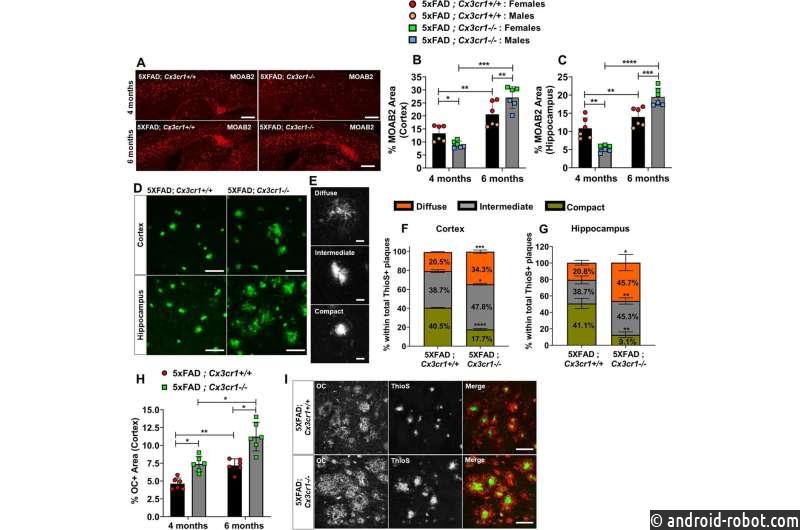
Исследование, опубликованное в журнале Molecular Neurodegeneration , показало, что удаление CX3CR1, микроглиального гена, связанного с нейродегенеративными заболеваниями , на животных моделях болезни Альцгеймера приводит к обострению болезненного состояния и накоплению бляшек в головном мозге . Дефицит гена также нарушил движение микроглии — иммунных клеток мозга — к бляшкам.
«Это исследование показывает, что микроглия при болезни Альцгеймера становится дисфункциональной на более ранних стадиях течения болезни в отсутствие CX3CR1, и эта дисфункция приводит к каскаду нейротоксических событий в головном мозге», — сказала Швета Пунтамбекар, MS, Ph.D., научный сотрудник. профессор медицинской и молекулярной генетики.
«Для более широкого исследовательского сообщества это исследование указывает, как мы можем воздействовать на этот тип клеток на ранних стадиях заболевания, чтобы модулировать прогрессирование заболевания в мозге и, в конечном итоге, модулировать когнитивные результаты при болезни Альцгеймера».
В прошлых исследованиях на людях и животных было показано, что CX3CR1 подавляется при нейродегенеративных заболеваниях, когда активируется микроглия. CX3CR1-V249I, вариант гена с потерей функции, был впервые идентифицирован и связан с дегенерацией желтого пятна, а позже было показано, что он связан с нейродегенерацией при болезни Альцгеймера и БАС.
Пунтамбекар, первый автор журнальной статьи, сказал, что в исследовании также рассматривалась связь между бета -амилоидом и тау-белком в мозге — характерными белками, обычно связанными с нейродегенеративными заболеваниями. Бета-амилоидные белки слипаются и образуют бляшки, которые разрушают связи нервных клеток. Позже тау может образоваться в мозгу после амилоидных бляшек .
«Исследование установило связь не только между амилоидом и тау, но и тем, как микроглия может формировать весь процесс заболевания», — сказал Пунтамбекар.
В отсутствие этого гена микроглия, выступающая в качестве первой линии защиты от вирусов, токсичных материалов и поврежденных нейронов, не может приближаться к бляшкам для очистки белков. Это происходит на ранней стадии заболевания и приводит к более нейротоксическим явлениям, таким как накопление других токсичных видов бета-амилоида и усугубление тау-белка на более поздних стадиях заболевания.
По словам Пунтамбекара, некоторые из этих видов бета-амилоида не откладываются в мозге в виде «нерастворимых» бляшек, а скорее накапливаются в мозге в виде растворимых бляшек, и было показано, что они также связаны со снижением когнитивных функций. Она добавила, что эти виды были увеличены в отсутствие CX3CR1.
Большинство методов лечения, нацеленных на бета-амилоидные белки в головном мозге, сосредоточены на нерастворимых бляшках, но в течение многих лет в клинических испытаниях было доказано, что лекарства неэффективны.
«С этим новым набором данных мы теперь можем начать задаваться вопросом, связана ли ограниченная клиническая эффективность терапии болезни Альцгеймера с тем, что не нацеливаются на правильные виды бета-амилоида, и должны ли мы начать нацеливаться на другие растворимые виды, чтобы получить лучшие когнитивные результаты», — сказал Пунтамбекар.