Гемостаз жизненно важен для предотвращения чрезмерной кровопотери. Однако существует повышенный риск тромбоза, если наблюдается чрезмерная реакция и неконтролируемое образование фибрина. В новом исследовании, опубликованном в журнале Nature Cardiovassal Research, исследовательская группа из Вюрцбурга под руководством Бернхарда Нисвандта обнаружила гликопротеин тромбоцитов GPV в качестве центрального регулятора гемостаза и образования тромбов, что открывает путь к новым терапевтическим подходам.
Когда наши кровеносные сосуды повреждены порезами, ссадинами или ушибами, жизненно важно остановить кровотечение и заклеить рану. Этот процесс называется гемостазом и включает два основных компонента: во-первых, тромбоциты прикрепляются к краям раны, образуют пробку и временно запечатывают рану. Во-вторых, инициируется свертывание крови или каскад коагуляции , что приводит к образованию длинных волокон фибрина, которые вместе с тромбоцитами плотно закупоривают рану.
Однако если фибрин образуется в избытке, например, при хронических ранах, могут возникнуть тромбозы и последующие закупорки сосудов. Поэтому важна строгая регуляция образования фибрина. До сих пор не было полностью понято, как ограничивается свертываемость крови.
GPV контролирует активность тромбина и образование фибрина
В этом исследовании исследовательская группа под руководством профессора Бернхарда Нисвандта выявила принципиально новый механизм. «Впервые нам удалось обнаружить новую точку переключения, которая регулирует как гемостаз, так и тромбоз. Этим переключателем является гликопротеин V, GPV, который экспрессируется на поверхности тромбоцитов. GPV контролирует активность фермента тромбина, который отвечает за образование фибрина», — объясняет Нисвандт, глава Института экспериментальной биомедицины I и член правления Центра Рудольфа Вирхова — Центра интегративного и трансляционного биоимиджинга (RVZ) в Университете Вюрцбурга.
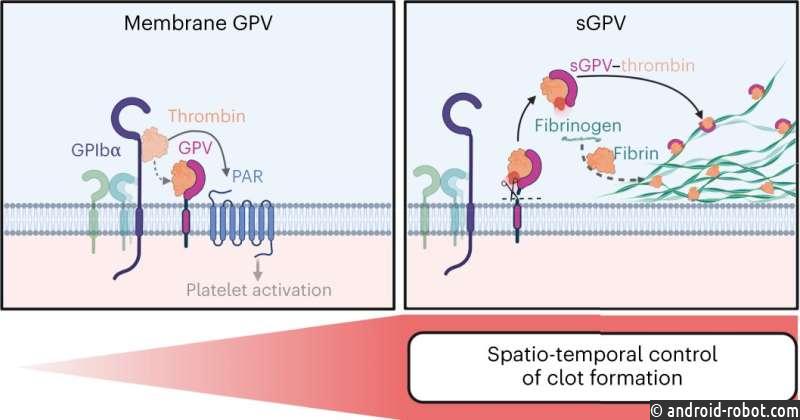
Тромбин является важнейшим ферментом свертывания крови , поэтому его активность необходимо точно контролировать в пространстве и времени. До сих пор было известно, что поверхностный рецептор ГПВ расщепляется тромбином при активации тромбоцитов. Это высвобождает GPV в виде растворимой формы.
Однако физиологическая функция этого рецептора была в значительной степени неизвестна. Используя генетический и фармакологический подходы, исследователи показали, что опосредованное тромбином расщепление GPV ограничивает образование фибрина. Оставаясь связанным с тромбином, растворимый GPV изменяет активность тромбина, так что он может образовывать меньше фибрина.
В экспериментальных моделях тромбоза было показано, что растворимый GPV предотвращает, среди прочего, образование вазоокклюзионных тромбов и приводит к значительной защите от экспериментального инсульта и связанного с ним повреждения головного мозга.
Бернхард Нисвандт убежден, что эти новые открытия изменят знания учебников. Он благодарит всех участвующих ученых из RVZ и Университетской больницы Вюрцбурга (UKW), которых поддержали коллеги из Майнца, Маастрихта и США.
Антитела против GPV обладают большим клиническим потенциалом в лечении нарушений гемостаза.
В другом подходе исследовательская группа создала антитела против GPV, которые предотвращают опосредованное тромбином расщепление GPV. «В наших исследованиях мы смогли показать, что эти антитела повышают активность тромбина, что приводит к повышенному образованию фибрина. Поэтому наша идея заключалась в том, чтобы использовать эти антитела в контексте нарушения гемостаза для увеличения образования фибрина», — говорит профессор Дэвид Стегнер, глава Группа визуализации сосудов РВЗ и один из последних авторов исследования.
В дополнение к генетическим причинам снижение количества тромбоцитов или нарушение функции также могут быть вызваны фармакологическим лечением и, следовательно, привести к нарушению гемостаза. Лечение ингибиторами агрегации тромбоцитов, такими как клопидогрел, которые используются для профилактики сердечных приступов или инсультов, а также для лечения нарушений кровообращения, ухудшает функцию тромбоцитов.
«В экспериментальной модели гемостаза наше новое антитело действительно было способно восстанавливать гемостаз в условиях, когда гемостаз в противном случае невозможен. Это указывает на поддержку гемостаза за счет усиления тромбин-зависимого образования фибрина», — добавляет доктор Сара Бек, научный сотрудник Вюрцбургский институт экспериментальной биомедицины и первый автор исследования. «Лечение против ВПЧ может иметь большой клинический потенциал. Это будет изучено более подробно в будущем».