Составляя более 78% воздуха, которым мы дышим, азот является элементом, наиболее часто встречающимся в чистом виде на земле. Причиной обилия элементарного азота является невероятная стабильность и инертность динитрогена (N 2 ), молекулы, содержащей два атома азота, и формы, в которой существует большинство азота. Только в очень суровых условиях, таких как ионосфера, диноген может быть собран в более длинные цепочки азота, образуя ионы N 4 с очень коротким временем жизни.
Несмотря на инертность диазота , природа способна использовать его в качестве важного сырья для всех видов живых организмов. В биологических системах очень сильная азотно-азотная связь в N 2 может быть расщеплена и может быть получен аммиак (NH 3 ), который затем становится источником азота для всей пищевой цепи на Земле.
Совершенно новая химическая реакция
Имитируя природу, люди используют важнейший процесс Хабера-Боша для расщепления азота до аммиака, который затем может быть переработан для производства удобрений и обеспечения доступности азота для производства пигментов, топлива, материалов, фармацевтических препаратов и других материалов. Получение соединений, которые содержат цепочки из двух, трех или четырех атомов азота, которые, в частности, имеют фармацевтическое значение в вазодилатирующих препаратах, требует повторной сборки молекул моноазота, таких как аммиак, поскольку не существует прямой реакции, которая могла бы напрямую соединить молекулы диоксида азота.
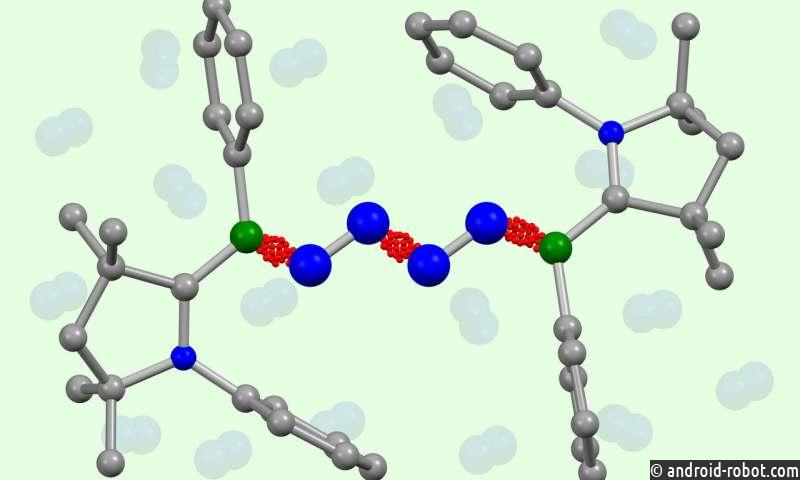
На этой неделе исследовательские группы из Германии из Университета Юлиуса-Максимилиана-Вюрцбурга (JMU) и Университета Гете во Франкфурте сообщают о совершенно новой химической реакции в журнале Science . Новый процесс использует борсодержащие молекулы для непосредственного соединения двух молекул N 2 в цепь N 4 . Впервые им удалось напрямую связать две молекулы атмосферного азота N 2 друг с другом без необходимости сначала расщеплять азот на аммиак, минуя процесс Хабера-Боша. Этот новый метод может позволить прямую генерацию более длинных цепочек азота.
Открывая путь новой химии
Новый путь синтеза функционирует в очень мягких условиях: при минус 30 градусах Цельсия и при умеренном давлении азота (около четырех атмосфер). Это также не требует катализатора переходного металла, в отличие от почти всех биологических и промышленных реакций азота.
«Это откроет путь химии, с помощью которой можно синтезировать совершенно новые молекулы азота в форме цепей », — говорит профессор химии JMU Хольгер Брауншвейг. Впервые азотные цепи, содержащие особый вариант азота (изотоп 15N), также могут быть легко получены.
Этот научный прорыв основан на экспериментальной работе постдока доктора JMU Марка Андре Легаре и кандидата наук Максимилиана Ранга.
Теоретическое понимание, предоставленное Университетом Гете
Кандидатура доктора Юлия Швейцер и профессор Макс Хольтхаузен из Университета Гете во Франкфурте отвечали за теоретическую часть работы. Они касались вопроса о том, как четыре атома азота химически связаны.
«С помощью сложных компьютерных симуляций мы смогли понять неожиданно сложные условия связывания в этих красивых молекулах. Это позволит нам предсказать будущую стабильность таких цепочек азота и поддержать наших экспериментальных партнеров в дальнейшем развитии их открытия, говорит профессор химии во Франкфурте.
Следующие шаги в исследовании
Исследовательские группы стремились включить новые молекулы азотной цепи в органические молекулы, которые имеют отношение к медицине и фармацевтике, особенно позволяя производить их аналоги 15N.