Являясь одним из 100 наиболее важных химических веществ в мире, перекись водорода (H 2 O 2 ) в основном производится энергоемким и затратным методом окисления антрахинона (AO). Замена метода AO более экологически чистой электрохимической двухэлектронной реакцией восстановления кислорода (2e — ORR) зависит от дешевых и эффективных катализаторов.
Катализатор на основе углерода, не содержащий металлов, как многообещающий кандидат, ведет себя обнадеживающе только в нейтральных или щелочных условиях, когда H 2 O 2 нестабилен для сбора или неблагоприятен для связывающих приложений, т. е. реакции Э-Фентона. Более того, по-прежнему сложно идентифицировать настоящие активные каталитические центры и лежащий в их основе механизм 2e- ORR .
В исследовании, опубликованном в журнале Chem Catalysis , исследовательская группа под руководством профессора Гуана Лунхуи из Фуцзяньского института исследований структуры вещества Китайской академии наук разработала не содержащий металлов высокоэффективный кислотный катализатор 2e- ORR с записанным водородом, скорость производства пероксида на основе модуляции активного центра с помощью пиримидина и S, N-содопированного малослойного графена для оптимизации валентной электроники.
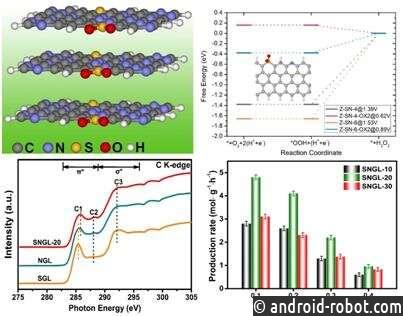
Катализатор показал исключительную активность и селективность в отношении 2e- ORR в кислоте. Селективность H 2 O 2 достигает 90%~100% в диапазоне потенциалов 0,20~0,55 В, а максимальная скорость образования H 2 O 2 (4,8 моль·г -1 ·ч -1 ) превышает все зарегистрированные значения H 2 O 2 . производительность катализаторов на основе углеродных материалов.
Эксперименты и моделирование теории функционала плотности (предоставленные профессором Чай Гуоляном) показали, что синергетический эффект комбинированного функционального мотива окисленной серы и пиридинового N может снизить уровень Ферми валентных электронных состояний активных краевых углеродных центров и, таким образом, приводит к к подходящей силе связывания промежуточного соединения *OOH для высокой селективности и производительности 2e — ORR для образования H 2 O 2 .
В частности, исследователи наблюдали очевидный сдвиг пика возбуждения C 1s в сторону высоких энергий в тонкой структуре поглощения рентгеновских лучей на ближнем крае с включением S, что является убедительным доказательством оптимизации валентно-электронной поверхности углеродного катализатора.
Кроме того, в сочетании с реакцией Фентона для электронно-фентоновского процесса он может разлагать модельный органический загрязнитель ( метиленовый синий [MB], 50 частей на миллион) до бесцветного за короткое время 15 минут.
Это исследование не только создает эффективный катализатор на основе углерода для производства H 2 O 2 в кислоте, но также обеспечивает полезный путь оптимизации электронных свойств для будущей настройки катализаторов на основе углеродных материалов.